

最近アメリカで冷凍シェイクが原因の食中毒が発生し、患者が7年間にも渡って発生していたというニュースを見たよ。
同じ菌がそんなに長く製品が汚染するのかな?
アメリカで発生したこの事件は、冷凍シェイクが原因で12人が亡くなったこと、そして7年間にもわたって同じ菌が製品を汚染し続けていたということで、アメリカでは大きな話題になっています。



このような長期間にわたる食中毒は、日本では聞いたことがありません。
WGS(全ゲノムシーケンシング)が食中毒調査で用いられていない日本では、このような「同じ菌が長期間にわたって製品を汚染し続け、食中毒が起きている」ことに気が付けない状況です。
しかし、このような「同じ菌が長期間にわたって食中毒を起こす」ことは、実は海外では時折起きています。(数か月続く食中毒であれば、サルモネラやリステリアで頻繁に起きています。)
そこでこの記事では、「長期間にわたって発生した食中毒の事例」と「その対策の考え方」について紹介します。



日本でいつ起きてもおかしくない事例です。日本の食品事業者の方はぜひ海外の事例を参考に対策を考えてみてください。
事例①:7年間患者が発生し続けた食中毒
まずは最近話題になっている「冷凍シェイク」を原因とするリステリア食中毒を紹介します。


| 患者数 | 38人 |
| 入院者数 | 37人 |
| 死亡者数 | 12人 |
| 年齢 | 43歳~101歳(中央値78歳) |
| 患者の発症日 | 2018年8月~2025年1月 |
| 患者の居所 | 21州 |
| 原因食品 | 冷凍シェイク飲料(栄養補助食品) |
| 原因菌 | リステリア(Listeria monocytogenes) |
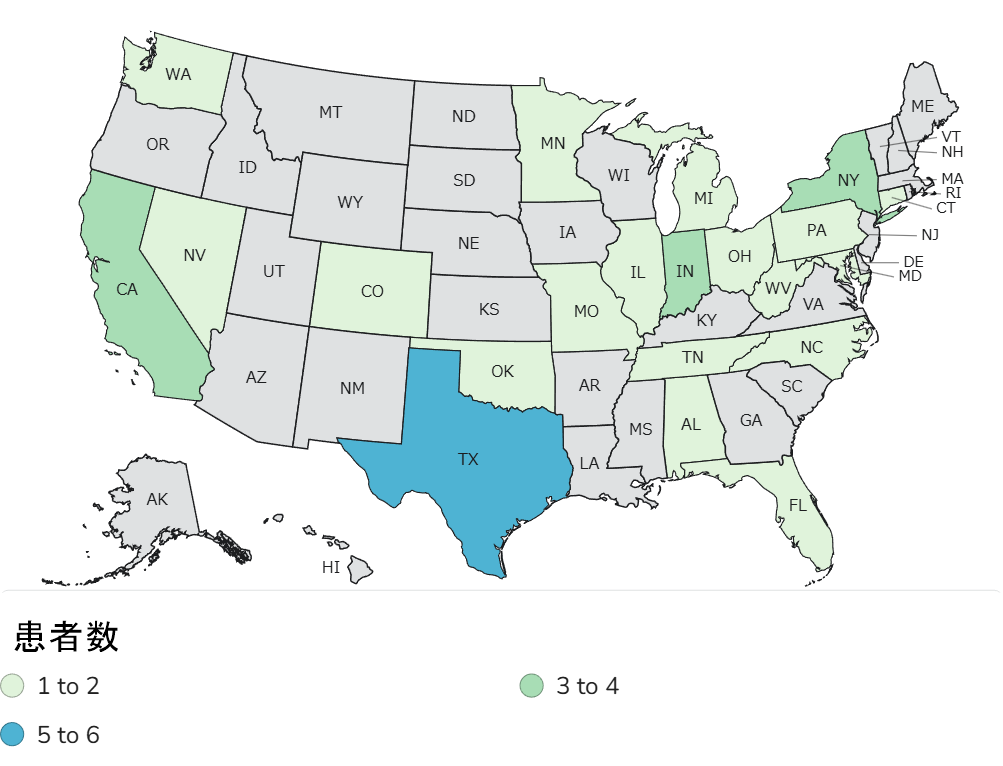

問題となった冷凍シェイクは、主に病院や介護施設向けに販売されていたもので、栄養補助食品として使用されたり、流動食が必要な人に対して提供されていたようです。
この製品はいわゆる「RTE食品」で、飲む前に冷蔵庫で解凍し、解凍後はよく振ってコップに注ぎ、そのまま飲むことができます。
※「RTE」はReady To Eatの頭文字をとったもので、加熱や調理をせずにそのまま食べられる食品を意味します。食べる前に加熱工程がないため、一度リステリアに汚染されると、食中毒を防ぐことが難しい食品です。
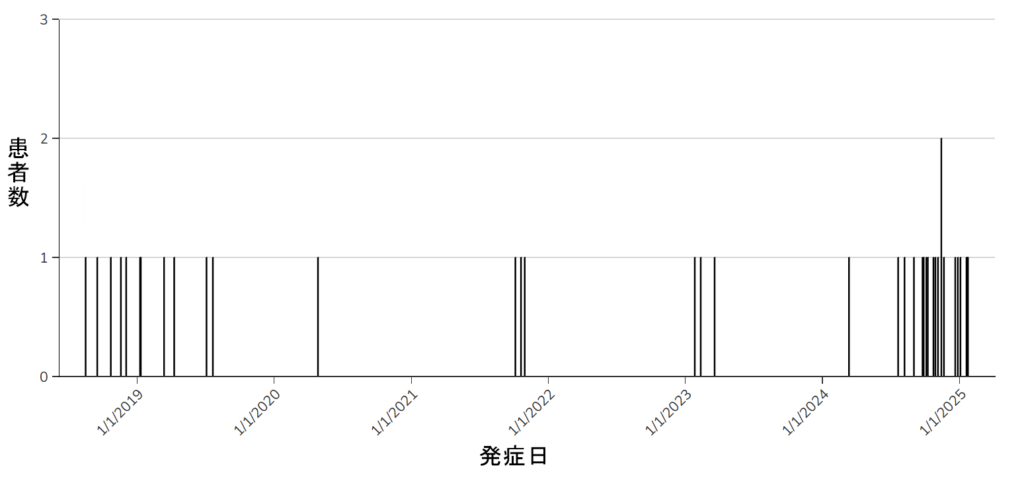

患者の発症日を見るとわかるように、2018年から断続的に患者が発生しています。そして、FDAやCDCは患者が発生するたびに食中毒調査を調査を行いました。
過去の調査では、患者の多くが介護施設や老人ホームの居住者で、そこで提供される食品が原因である可能性が高いということはわかっていましたが、原因食品の特定までには至りませんでした。



リステリア食中毒の調査は、他の食中毒と比べて特に原因食品の特定が難しいと言われています。
2024年になって再び多くの患者が発生したため、2024年10月から再度調査が行われました。
今回の調査では、患者が比較的短期間に多く発生していたため、患者への聞き取りや、介護施設の納品伝票を確認することで、「疑わしい食品」(冷凍シェイク)を見つけ出すことができました。


2025年2月にはFDAが冷凍シェイクを製造した工場に立ち入りを行い、工場の環境ふき取り検査を行いました。
すると、患者から検出されたリステリアと遺伝的に同一のリステリアが検出され、この工場で作られた「冷凍シェイク」が食中毒の原因であると特定されました。



「何が問題でシェイクがリステリアに汚染されたのか」や「工場ではリステリアに対しどのような対策をとっていたのか」などは、現在調査中のため、今後FDAから詳細が発表されることに期待です。
事例②:10年後に再び起こった食中毒
2008年に起こった食中毒
次はシリアルが原因となったサルモネラによる食中毒です。
| 患者数 | 33人 |
| 入院者数 | 12人 |
| 患者の発症日 | 2008年1月~7月 |
| 患者の居所 | 17州 |
| 原因食品 | 米シリアル、小麦シリアル(Puffed wheat and rice cereals) |
| 原因菌 | サルモネラ(Salmonella Agona) |


2008年4月頃に同じタイプのサルモネラが複数の患者から検出されていることを探知し、調査が開始されました。
その後、FDAがこのシリアルを製造していたミネソタ州にあるX社の工場に立ち入り、製品の検査、環境ふき取り検査を行ったところ、患者から検出されたものと同じ「Salmonella Agona」を検出しました。
このシリアルの製造工程では、米や小麦を膨らませるために「puffing gun」が使われており、この加熱により、病原菌の殺菌が行われていました。



「puffing gun」はこちらの動画の最初の30秒を見てもらえればイメージがつかめると思います。ポン菓子を作るのと同じ原理です。
その後、不純物を除去する工程があり、製造室の床付近にある通気口から空気を吸引することで、ほこりや膨らんでいない粒などの異物を除去していました。
そしてFDAの担当者たちは、この製造室の壁の一部が壊されていることを発見しました。


工場によると、2007年11月にメンテナンス作業のために壊したとのことでした。



この「壊された壁」が今回の食中毒発生と大きく関わっていました。その謎を知るには、10年前にさかのぼる必要があります。
1998年に起こった食中毒
1998年にオーツ麦シリアルを原因食品とするサルモネラ食中毒が発生しました。
| 患者数 | 209人 |
| 入院者数 | 47人 |
| 患者の発症日 | 1998年4月~5月 |
| 患者の居所 | 11州 |
| 原因食品 | オーツ麦シリアル |
| 原因菌 | サルモネラ(Salmonella Agona) |
患者調査により「オーツ麦シリアル」が原因と突き止められました。
実は、この製品は2008年に発生した食中毒と同じミネソタ州にあるX社の工場で製造されていました。
FDAがこの工場に立ち入り、製品検査、環境ふき取り検査を行ったところ、患者から検出されたものと同じ「Salmonella Agona」が検出されました。



同じ施設で1998年と2008年に同じ菌が検出されたのですね!
1998年当時の調査では、「Salmonella Agona」の発生源を特定することはできませんでした。
そのため、この食中毒の対策として、製造施設の汚染された区域を封鎖するために、全ての機器を撤去し、壁の表面をむき出しのコンクリートまで剥がし、菌の除去を行い、エポキシ樹脂で再仕上げを行いました。


この対策により、1998年の食中毒はとりあえず終息しました。
そして、再び2008年です。
2008年に食中毒が発生する前年の2007年に、メンテナンス作業で封鎖された区域のすぐ隣の壁を開ける必要がありました。
そして、メンテナンス作業中に壁を破壊した際の粉塵、この区域の洗浄に用いられた水によって、「Salmonella Agona」がシリアル製造区域に運ばれたと考えられています。



つまり、2007年11月にメンテナンス作業のため壁が壊されたことで、10年前に封じ込めた「Salmonella Agona」が再び工場を汚染してしまったのですね。
加熱工程後の不純物を除去する工程では、床付近に空気の吸気口がありました。
そして、その吸気口の近くにあった排水口の湿った状態が、「Salmonella Agona」の生存・増殖を促進し、包装直前のシリアルを汚染したと考えられています。
2008年の食中毒の後にX社は問題となったシリアルの製造を永久に中止し、工場のこの区域を食品製造に使用することを停止しました。



この食中毒の教訓は、根本原因を解決しないと同じ問題が再発してしまうこと、乾燥下において何年も生存できるサルモネラの乾燥耐性を見誤っていたこと、そして工事やメンテナンスは微生物汚染が起きる絶好の機会だということです。
根本原因分析、サルモネラの乾燥下での生存能力、工事のリスクについては下の記事をご覧ください。






一過性 VS 定着性



長期間にわたって同じ菌が原因で食中毒が起きることはわかったけど、どのように対策すればよいのだろう?



食品営業施設に存在する病原菌のパターンを次の2つわけて、それぞれに対する対策を考えましょう。
一過性の病原菌(transient pathogen)
「一過性の病原菌」は、環境ふき取り検査で病原菌(例えばサルモネラやリステリア)が検出されても、次回以降のふき取り検査では検出されない場合です。
次回以降のふき取り検査で陰性となる理由は次の2つが考えられます。
- 病原菌が存在しても検出できなかった場合
- そもそも病原菌が存在しなかった場合(自然にいなくなった、洗浄消毒で除去できた)
1はサンプリング方法や検査感度の限界により、菌が検出されないということです。そのため、「検査精度」という別の問題になります。
そのため「一過性の病原菌」は2のことを指します。
つまり、「一過性の病原菌」は一時的に病原菌が施設に侵入しても、定着せずに自然消滅、もしくは洗浄・消毒により除去できたケースです。


定着性の病原菌(resident pathogen)
「定着性の病原菌」は、環境ふき取り検査で病原菌が検出され、その後の検査でも「同じ病原菌」が検出される場合です。
つまり、病原菌が施設に「定着」してしまったということです。



参考までにFDAは、60日以上経った後のふき取り検査で、再度同一の菌を検出した場合を「定着性の病原菌」と分類しています。
定着性の病原菌は、洗浄・消毒が難しい場所(ひび割れ、構造物の接合部、排水溝、穴など)に定着します。
このような場所は、食品の残渣や水分が蓄積しやすく、病原菌が増殖、生存しやすい環境にあります。
さらに、バイオフィルムが形成されると、熱、乾燥、消毒などに対して、病原菌の耐性が高まります。
また、サルモネラやリステリアは乾燥した環境や食品中でも長期間にわたって生存することができます。
つまり、洗浄消毒が行き届かない場所、水分や食品残渣が溜まりやすい場所、乾燥した場所に病原菌が定着してしまうケースです。



どうして病原菌を「一過性」と「定着性」に分ける必要があるのですか。



病原菌が検出された場合の対応が違ってきます。
「一過性」であれば、通常の一般衛生管理(施設の洗浄・消毒を行う、従業員教育を行うなど)を行うことで、病原菌を除去できます。
一方「定着性」の場合、その汚染源は施設で通常行う対策では、効果が届きにくい場所にいます。
そのため、「定着性の病原菌」に対して「一過性の病原菌」と同じ対策を行っても、問題が解決されません。
「定着性の病原菌」の発生源を特定するためには、徹底的な調査(根本原因調査)と原因に対する対策、そして定期的なモニタリングが必要になります。



食品工場では、実際どれくらいの病原菌が一過性なのか、定着しているのかデータはあるのですか?
FDAが立ち入った536施設で行った環境ふき取り検査の結果を分析したところ、21%が定着性の病原菌でした。
そして、最長でサルモネラでは10年近く、リステリアでは12年以上、同じ菌が検出されました。



このように、定着した病原菌への対策を取らなければ、長期間にわたって、製品を継続的に汚染する恐れがあります。
FDAが2025年1月に公表した「水分活性が低いRTE食品向けの衛生プログラム及び是正措置のガイドライン案」では、環境ふき取り検査から病原菌を検出した場合に、その菌の型別試験を行うことを推奨しています。
型別試験とは、血清型、PFGE、WGSなどの試験を行い、その病原菌の種類をより詳細に知ることがです。
そして、ガイドライン案の中では、型別試験の中で最も解像度が高い「WGS」を行うことが推奨されています。



WGSを用いることで、遺伝的に同一の菌かどうかを知ることができます。そのため、自信を持って「一過性」なのか「定着性」なのか判断することができるということです。
PFGE、WGSについて知らない方は下の記事をご覧ください。


おわりに
以上が長期間にわたって同じ菌が原因で発生した食中毒事例とその対策の考え方です。
本来であれば「このような食中毒が起きないようにする」、「起きたとしても迅速に汚染された食品を特定できるようにする」ことが必要です。



それにはどうすればよいのでしょうか?
解決策の一つとしては、食品の生産から消費に至るまでのすべてのWGSの検査結果を1つのデータベースに集めることです。
生産者の水や土壌、農産物の検査結果、食品事業者や行政機関が行っている製品検査や環境ふき取り検査の結果、患者から検出した病原菌の結果をすべて同じデータベースにアップロードします。
そして、これらのWGSの結果と患者から検出した菌の結果が一致すれば、食中毒の原因食品と患者を瞬時につなげることができます。
まるで夢物語のような話ですが、実は上記の内容はアメリカの「GenomeTrakr」という取組の説明で、成果も出ています。



今後、全世界で「GenomeTrakr」のような取組が活用されることで、食中毒起きてもすぐに解決される世の中が来るかもしれません。










コメント
コメント一覧 (2件)
[…] 洗浄後は陰性になっても、またしばらくすると検出したことから、サルモネラが施設に定着していたのですね。 […]
[…] もしかすると、ずっと以前から汚染されていた可能性もあるのですね。 […]